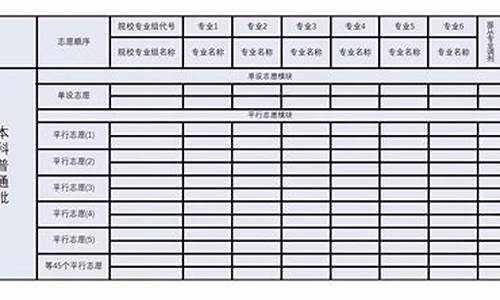
2012年北京高考化学,2013北京高考化学解析
1.高考化学
2.2011北京高考理综化学27
3.高考化学第十四题
4.求此题解析 高考化学

一、明确任务
一轮复习基本是按知识模块与课本的章节顺序综合,梳理知识细节、构建知识网络,而二轮复习则是按照模块化、程序化的方式进行综合训练,所以二轮复习节奏更快、强度更高。
二轮复习的主要任务,一是形成知识网络系统并强化记忆。二是在系统把握整体知识的基础上,通过大量练习,培养学生综合灵活运用知识的学科能力。解题的过程中,注意提高速度及准确性。做到既要?对?,又要?快?。
二、具体建议
二轮复习主要是通过练习强化对知识的理解和应用。综合训练与专题训练相结合,练题的同时注意归纳总结,比如有机推断专题,钢铁的腐蚀、离子反应等专题。同时,训练答题的准确性、规范性,提高解题速度,多整理易错点、失分点,并进行强化练习。信息题则要学会如何去粗取精、去伪存真。以下列举三点具体建议:
1、专题训练、归纳总结
近几年的高考化学试卷,逐年倾向于?能力立意?,更加注重能力和素质的考查。同时由于试题数目有限,高考卷考察的知识点也比较固定。所以专题练习可以按照题型和知识点分类专题练习。以北京高考题为例,7道选择题中,电化学(原电池、电解池或者金属的防护和腐蚀)、化学反应速率和平衡、方程式的正误判断、实验题是常考题目,我们就可以按照这样的专题进行练习。练习时,注意归纳总结,反思复习,找出同一类题目之间的共通点,同时构建知识点之间的联系,形成完整的知识体系,以题目?反刍?知识,以知识指导题目。
2、限时训练、综合训练
(1)限时训练
理综化学的选择题并不多,北京卷7道, 考试时10-15分钟内完成比较合适,建议学生给自己规定一个时间,对每一个专题模块或者综合训练时进行限时训练,防止大量题海战术时脑疲劳,做题效率下降。
(2)综合训练
每周进行一次学科内综合训练。以北京卷为例,7道Ⅰ卷选择题,4道Ⅱ卷题,限时45分钟完成。45分钟时间虽然紧张,但不能给得太多时间。此用意在于:①提高解题速度;②提高阅读、审题能力;③学会合理舍弃,同时调整考试心理,提高考试技巧。
3、跳出题海、突出方法
由于复习时间紧任务重,要使学生在有限的时间内复习掌握大量知识并形成知识网络,就必须跳出题海,突出方法,提高复习效率。突出主干知识相关的题目和题型,新题、难题、偏题适当舍弃。注意建立知识之间的练习,注重对思维能力的训练,注重对学习方法归纳,并留出时间思考和通读课本。
解题时有意识地进行思维能力训练,找出该题所涉及的知识点(审题)?回忆、联想相关的知识(构思)?应用知识点解决问题(解答)。要注意无论专题训练还是综合训练,都必须目的明确,落到实处,重在效果,达到训练几道题通晓一类题的目的,切忌贪多求全,题海战术,疲于奔命。
高考化学
(1)NaOH (2)2Cl-+2H2O2OH-+H2↑+Cl2↑
(3)Cl2与水反应:Cl2+H2OHCl+HClO,增大c(HCl)使平衡逆向移动,减少cl2的溶解度,有利于cl2的产生。
(4)①Mg(OH)2 ②2NH4++3Cl2+8OH-=8H2O+6Cl-+N2↑
③SO42-、Ca2+ ④1.76kg
2011北京高考理综化学27
解析
试题分析:(1)燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,甲醚的燃烧热为1455 kJ/mol,则甲醚燃烧的热化学方程式为CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) △H= —1455kJ/mol;已知H2(g)和C(s)的燃烧热分别是285.8 kJ·mol-1、393.5 kJ·mol-1,则有关的热化学方程式为:①H2(g)+1/2O2(g)=H2O(l)△H=-285.8KJ/mol;②C(s)+O2(g)=CO2(g)△H=-393.5KJ/mol;③CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455kJ/mol,所以根据盖斯定律可知①×3+②×2-③得到反应热化学方程式为:2C(s)+3H2(g)+1/2O2(g)=CH2OCH3(g) △H=-169.4kJ/mol,即4C(s)+6H2(g)+O2(g)=2CH2OCH3(g) △H=-378.8kJ/mol;
(2)①在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A、氢气是反应前,水蒸气是生成物,因此当c(H2)与c(H2O)的比值保持不变时可以说明反应达到平衡状态,a正确;b、根据方程式可知单位时间内有2mol H2消耗时一定有1mol H2O生成,因此不能据此说明达到平衡状态,b错误;c、密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此容器中气体密度不再改变不能说明达到平衡状态,c错误;D、正方应是压强减小的可逆反应,因此当容器中气体压强不再改变是能说明达到平衡状态,d正确,答案选ad。
②正方应是放热反应,因此温度升高,该化学平衡向逆反应方向移动,到达新的平衡,CH3OCH3的产率将变小。混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,物质的量增大,则混合气体的平均式量将变小。
(3)原电池负极失去电子,发生氧化反应。因此甲醚在负极放电,碱性条件下生成碳酸根离子与水,则电极反应式为CH3OCH3+16OH-—12e-=2CO32-+11H2O;
(4)根据装置图可知Y电极与电源的正极相连,作阳极。溶液中的氯离子放电生成氯气,因此Y电极附近溶液中有气体产生,上部分呈黄绿色;标准状况下2.8LO2的物质的量是2.8L÷22.4L/mol=0.125mol,根据电极反应O2+2H2O+4e-=4OH-可知电子转移为0.125mol×4=0.5mol。所以根据电子守恒可知电解池中也转移0.5mol电子,因此根据阳极电极反应为4OH--4e-=2H2O+O2↑可知生成氢氧根离子的物质的量是0.5mol,其浓度是0.5mol÷0.5L=1.0mol/L,所以溶液中氢离子浓度是10-14mol/L,因此溶液的pH=14。
考点:考查燃烧热、热化学方程式、盖斯定律、平衡状态判断、外界条件对平衡状态的影响以及电化学原理的应用等
答案
(1)CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) △H= —1455kJ/mol(2分)
△H=—378.8kJ/mol(3分) (2)①a d;(各1分,共2分)②变小;变小;(各1分,共2分)
(3)CH3OCH3+16OH-—12e-=2CO32-+11H2O(2分)
(4)Y电极附近溶液中有气体产生,上部分呈黄绿色(2分) 14(2分)
高考化学第十四题
二氧化硫气体是无法使氯化钡产生沉淀的,但是甲的方案只是排除氧气的存在保留酸雾的存在,而酸雾溶于水就会产生硫酸根离子,从而与氯化钡产生硫酸钡沉淀
酸雾的成分应该是SO3 ·nH2O
求此题解析 高考化学
答案选择B。
解析:1. 化学键包括了离子键,共价键和金属键. H2O中的氢,氧原子还会形成氢键,氢键不是化学 键,所以1错
2. MnO4- 中的Mn与O形成的是共价键,所以2错
3 离子键(ionic bond)指阴离子,阳离子间通过静电作用形成的化学键,所以3错
4. HCl 间形成的是共价键
5. 反应过程是H2,Cl2 中的共价键断裂生成H,Cl原子,然后H,Cl原子形成共价键的过程,所以5错
故答案选B
1、a、c一开始体积、压强都相等,反应物的量也一样,刚开始的速度自然就一样。
2、由于c是活塞,随着反应的进行,c容器的体积减小,反应物的密度与原先一样。反应一段时间后,a容器中反应物的密度减小,分子距离变大,反应速率也就慢了。
3、注入氮气,不会影响反应,但会影响容器的压强。a、b都是定容,a的压强就比b大,而c有活塞的调节,压强依然与原先相同;起始反应速率由于a、b体积不变,速率也就相等,c的体积在如氮气后增大了,反应物密度减小,反应速率就小。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。