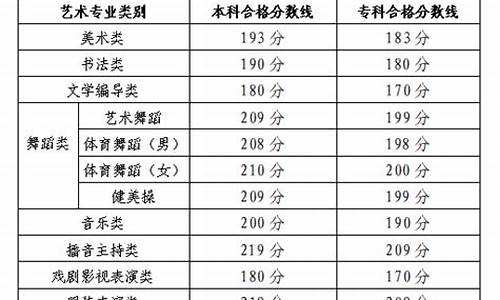
2017高考二卷理综答案解析,2017高考理科二卷答案

26.(14分)水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__________,还可使用___________代替硝酸。
(2)沉淀A的主要成分是_________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_____________。
(3)加氨水过程中加热的目的是___________。沉淀B的主要成分为_____________、____________(填化学式)。
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:MnO4-+H++H2C2O4→Mn2++CO2+H2O。实验中称取0.400 泥样品,滴定时消耗了0.0500 mol·L-1的KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为______________。
答案:
(1)将Fe2+氧化为Fe3+?;?双氧水
(2)?SiO2?;SiO2+4HF=SiF4↑+2H2O
(3)促进Fe3+、Al3+水解;Fe(OH)3?、 Al(OH)3
(4)?5Ca2+~5H2C2O4~2KMnO4
n(KMnO4)=0.0500mol/L×36.00mL=1.80mmol?n(Ca2+)=4.50mmol
水泥中钙的质量分数为4.50mmol×40.0g/mol/0.400g=45.0%
解释:因为一般情况下Mg2+开始沉淀需要pH>8.
金属离子:沉淀形式,开始沉淀pH,完全沉淀pH
Mg2+:Mg(OH)2,8.10,9.43
Fe3+:Fe(OH)3,1.47,2.80
Al3+:Al(OH)3 ,4.20,5.37
3cosa+4sina可以取值+/-5,在第三象限应为-5,因此-5-4-a=+/-17,解得a=-26/8;综合得a=-16,-26,8,18四个值。
参考答案为-16,18.只取第一象限点了
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。